
" 実現力 " のケアティスです

フォールディング
(折り畳み)
(ぺプチジルプロリルイソメラーゼ)
(イムノフィリン)
(シクロフィリン)
(FK506結合タンパク質)
パルブリン : 原核生物
ケアティスがバイオ・メディカル分野における研究テーマの一つとして、シクロフィリンがあります。
ケアティスが考える実用化の展望について、上記「シクロフィリン概要図」を基に、不定期で連載する予定です。
第1回予定:ぺプチジルプロリルイソメラーゼ( PPlase )、シャペロンとは?
第2回予定:シクロフィリンA
第3回予定:シクロフィリンD
シクロフィリンとは?
シクロフィリンは、臓器移植で使用される免疫抑制剤のシクロスポリンが結合するタンパク質に因んで名づけられた
タンパク質でぺプチジルプロリルイソメラーゼ(PPlase)活性を有しています。
このPPlaseは異性化酵素(イソメラーゼ)の一種で、全ての生物に存在し、タンパク質分子中のプロリン残基のシス・トランス異性化を触媒します。
ぺプチジルプロリルイソメラーゼ(PPlase)とは?
アミノ酸間のペプチド結合は、一般にトランス体がシス体に比べて遥かに安定で、この状態が自然に達成されます。
ところがプロリン残基ではその特異な構造により、N側ペプチド結合がシス体としても比較的安定に存在します。
シクロフィリンのPPlase活性を測定する時の基質
Ala-Ala-Pro-PheのMolviewで作成した構造式です。
タンパク質の様な高分子では、シス・トランス体で、
より大きな構造的差異が生じます。
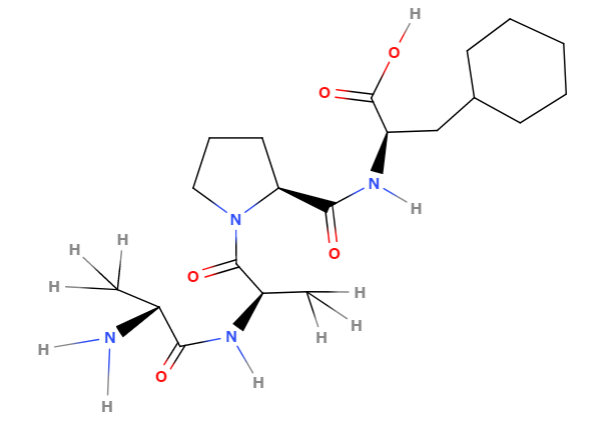
シス
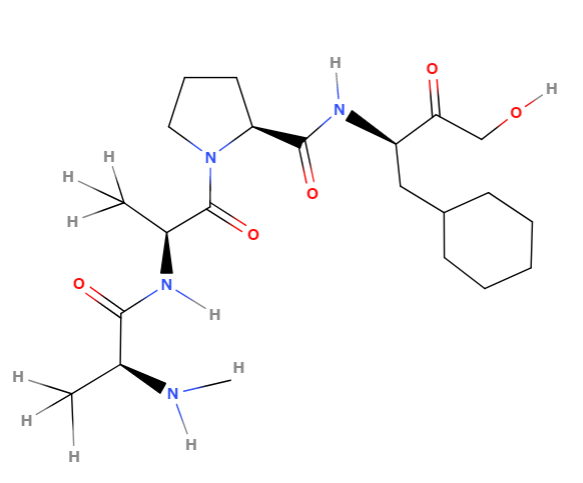
トランス
こちらはAla-Ala-Pro-Pheを静電ポテンシャルマップで
電子密度を示した動画です。ご覧ください。
生物の個体や細胞等の主要な構成分子であるタンパク質はアミノ酸からできていますが、タンパク質が正しく機能するためには
タンパク質の正確なフォールディング(折り畳み)が必要がです。
この結合のシス・トランス異性化に必要な活性化エネルギーは約20kcal/molと比較的高いので、この結合は自然には異性化しにくく、フォールディングには
プロリン残基の異性化が触媒される必要があります。
プロリルイソメラーゼはここで働きますので、シャペロンの一つということができます。
プロリルイソメラーゼの例としては、真核生物のシクロフィリン、FKBP、Pin1、原核生物のパルブリン等があります。
プロリルイソメラーゼは同じ種類のタンパク質に対しても活性があり、自己フォールディングを促進します。
シクロフィリンとFKBPはそれぞれある種の免疫抑制剤の標的タンパク質でイムノフィリンと総称されます。
これらは免疫系の調整で中心的な役割を果たすカルシニューリン等、シグナル伝達に関わるいくつかのタンパク質複合体の活性発現に必要ですが、
免疫抑制剤と複合体を形成すると逆にこれらタンパク質複合体を阻害することもあります。但し、この性質には、プロリルイソメラーゼ活性が直接関与しない可能性もあります。
次に、シャベロンについて説明します。
シャペロンとは?
他のタンパク質分子が正しい折り畳み(フォールディング)をして機能を獲得するのを助けるタンパク質の総称です。
分子シャペロン、タンパク質シャペロンともいいます。
シャペロンはあくまでネイティブ構造の形成がなされやすい環境、または機会を提供するだけですが、シャペロンの機能はフォールディングの補助だけではなく、
タンパク質の品質管理(複合体形成、輸送、リフォールディング、脱凝集)も担っています。
これらの機能は生命活動において必須事項であるため、シャペロンは必要不可欠な存在です。
分子シャペロンの異常は、細胞の恒常性維持に関わるタンパク質の機能不全を引き起こします。具体的には、代謝系の異常、腫瘍の進行、神経変性疾患、
心血管障害などの病気の進行の要因となると考えられています。
また、別の見方をすれば、細胞内に存在する個々のタンパク質のコンホメーション、結合相互作用、局在および濃度の制御(タンパク質恒常性)が適正化
かつ維持されるためにはシャペロンは必須の要素とも言えます。
シャペロンは以下の様に分類されます。
熱ショック対応
多くのシャペロンは熱ショックタンパク質(HSP)であり、温度の上昇による損傷を抑制するための熱ショック応答を担います。つまり
タンパク質のフォールディングが熱によって変性した場合に、そのタンパク質の折り畳みを適切になるよう制御します。
低温ショック応答
低温ショック応答を担うRNA結合性シャペロンの一群を低温ショックタンパク質(Csp)(RNAシャペロン)と呼びます。Cspは、RNA上に生じた余分な二次構造を
一本鎖状にほどき、遺伝子発現とタンパク質合成を可能にします。
新生タンパク質のフォールディング
ほとんどのタンパク質はシャペロンなしでも折りたたまれますが、一部にはシャペロンを必須とするものもあります。翻訳を経て新規合成されたばかりの
ポリペプチド鎖のフォールディングに限定すれば、シャペロンが必要なタンパク質は、細胞内タンパク質の30%に及ぶそうです。
新生ポリペプチド鎖の多くがシャペロンを必要とする理由は、作られたばかりでは疎水性のアミノ残基は周囲の水分子に露出しており(天然体では疎水性残基は内部にあり、
周囲の水分子から隔離されている)、水分子から逃れるために最初に遭遇した他の疎水性残基と結合しようとするためだそうです。最も近くの疎水性領域は本来の結合相手でない場合が多く、
手当たり次第の相互作用は間違ったフォールディングを導くそうです。こうしてフォールディングに失敗したタンパク質は凝集する傾向があり、凝集したタンパク質は細胞にとって非常に有害である
(例としては牛海綿状脳症の原因であるプリオンタンパク質や、アルツハイマー病の原因となるβアミロイドタンパク質など)ことが多い様です。
シャペロンは、正しい結合相手が現れるまで新生ポリペプチドの疎水性部分を水分子から隠す働きを持ちます。通常のシャペロンは、内部が疎水性領域となっているポケットを
持ち、ここに基質を格納します。基質の疎水性領域はポケット内の疎水性領域と相互作用し、不適切な結合は抑制されます。
ヒストンシャペロン
ヒストンシャペロンとは、ヒストンを裸のDNAに結合させてヌクレオソームを形成させるタンパク質です。このタンパク質の役割は、転写の際に一次的にクロマチン上
からヒストンが取り除かれて不安定化したヌクレオソームを元通りにすることです。この不安定化は、RNAポリメラーゼがヌクレオソーム内部の転写領域に接触して転写を行うために実行されていると考えられていて、ヒストンシャペロンとして、
クロマチン転写促進因子(FACT)が知られています。
(「シャペロンについて」は、Wikipediaのシャペロン(https://ja.wikipedia.org/wiki/シャペロン)から引用しました。)
シクロフィリンA
シクロフィリン(CyP)は、シクロスポリン(シクロスポリンA)に結合する能力に因んで名づけられたイムノフィリンファミリーです。
細胞質中に遍在的に分布するタンパク質です。複合体はカルシウム/カルモジュリン依存性ホスファターゼ、(カルシニューリン)の活性を阻害します。
CyPAは、ぺプチジルプロリルシス-トランスイソメラーゼ(PPIase)活性を持ち、タンパク質の折り畳みと輸送を調節します。
また、シクロフィリンA-シクロスポリン複合体の主要な働きとして、カルシニューリン活性を阻害することによって、前炎症物質であるTNF-αやインターロイキン2の産生をを抑制し、
移植臓器拒絶反応を抑制すると考えられています。
CyPAは当初、主に細胞内タンパク質として機能すると考えられていましたが、最近の研究では、CyPAは炎症性刺激に応答して細胞から分泌されることも明らかになっています。
動物モデルとヒトでの現在迄の研究で、いくつかのヒト疾患におけるCyPAの重要な機能を裏付ける証拠が出てきています。以下の表にまとめました。
| 疾患 | 根拠 |
 心臓病 心臓病 |
CyPAは心肥大、心虚血、および再灌流障害の重要な決定要因であり、冠動脈疾患の有用なバイオメーカーである可能性があります。 |
 ウイルス感染症 ウイルス感染症 |
CyPAはHIVカプシドタンパク質と相互作用することが明らかになりました。 CyPAはM1タンパク質の分解を促進することにより、インフルエンザウイルスの複製を阻害します。 CyPAはヌクレオカプシドタンパク質への結合と粒子への取り込みを介して、重度急性呼吸器症候群コロナウイルス(SARS-CoV)の複製を調節します。 |
 がん がん |
CyPAは ①がんの増殖を助ける(p53やHIFα) ②細胞周期の進行を調節する ③アポト-シスをブロックする ④細部の移動/浸潤を促進すること からがん細胞の増殖、転位、薬剤耐性に関与することが示唆されています。 |
| CyPAによる血液脳開門(BBB)の崩壊が核因子カッパB(NF-κB)およびMMP-9の活性化による炎症惹起を誘発することが知られています。 | |
 慢性関節リウマチ(RA) 慢性関節リウマチ(RA) |
RA患者では、細胞外液で分泌型のCyPAが確認されています。 CyPAは、変形性膝関節症患者と比較してRA患者の滑液で増加していることが知られています。 |
| 健康な歯肉組織と比較して炎症を起こした歯肉組織ではCyPA発現が劇的に上昇し、浸潤マクロファージ及びリンパ球や破骨細胞及び骨芽細胞に局在していることが知られています。 CyPAは、浸潤細胞及び/または炎症を起こした歯肉結合細胞の細胞マトリックスに局在していることが知られています。 CyPAは、PBMC/好中球の走化性とTNFα/IL-8の分泌を誘導することにより、歯肉組織の炎症に関与していることが示唆されています。 |
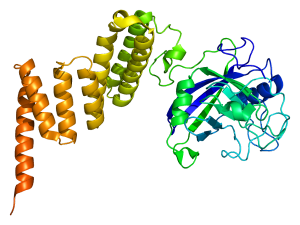
シクロフィリンDはミトコンドリアのマトリックスに存在し、ミトコンドリアの透過性遷移ポア(MPTP)の構成成分と考えられています。
例えば、虚血性脳障害では虚血という刺激によって一過性に細胞内のカルシウム濃度が上昇し、それが引き金となってMPTPが開き、クリステから
アポトーシスを透発するチトクロームCが細胞質内に放出されます。シクロスポリンはシクロフィリンDに結合し、MPTPの開放を抑制します。